This product was successfully added to cart!
品牌商品推荐
更多 >>商品详情
客户评价
| 描述 |
Osajin是 Maclura pomifera 果实中存在的主要生物活性异氟烷,具有抗肿瘤,抗氧化和抗炎活性。 |
||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 相关类别 |
|
||||||||||||
| 靶点 |
Apoptosis[1]
|
||||||||||||
| 体外研究 |
Osajin以剂量依赖性方式显着降低人NPC细胞(TW076,CG1和TW04细胞)的活力。 Osajin通过多种凋亡途径诱导人NPC细胞凋亡,包括外在死亡受体途径,以及依赖线粒体和内质网应激的内在途径[1]。 Osajin对六种人类癌细胞系具有生长抑制活性,包括肾,肺,前列腺,乳腺癌,黑色素瘤和结肠癌细胞[2]。 |
||||||||||||
| 体内研究 |
Osajin和pomiferin可减轻缺血再灌注引起的心肌功能障碍。抗氧化酶值和总抗氧化活性的增加证实了这一点。 osajin和pomiferin治疗提供的心脏保护作用来自抑制氧化应激,这与改善的心室功能相关[3]。 |
||||||||||||
| 溶解度 |
体外:
在DMSO中10mM
|
||||||||||||
| 储备液 |
|
||||||||||||
| 细胞实验 |
将NPC细胞接种在96孔板(5000个/孔)中并使其粘附24小时。然后用含有不同浓度(0.01-10μM)osajin的新鲜培养基替换培养基另外24小时。对于时程测定,5μMosajin的孵育时间为6,12,24,36和48小时。温育后,向每个孔中加入10μl5mg/ ml的MTT,并在37℃下孵育4小时。使用基于MTT的测定确定细胞活力[1]。 |
||||||||||||
| 动物实验 |
大鼠[1] Wistar大鼠分为四组。第一个治疗组接受osajin(5%/ kg /天,0.5%Avicel);第二治疗组接受pomiferin(0.5 mg Avicel中5 mg / kg /天);安慰剂组仅获得0.5 Avicel;最后一个是未经治疗的对照组。评价氧化损伤的生化指标 – 脂质过氧化产物丙二醛,抗氧化酶 – 超氧化物歧化酶,谷胱甘肽过氧化物酶,血清和心肌中的总抗氧化活性。研究了osajin和pomiferin对心功能,左心室舒张末压,左心室压力和峰值阳性+ dP / dt缺血再灌注的影响[1]。 |
||||||||||||
| 存储 |
请将产品存放在分析证书中的建议条件下。
|
||||||||||||
| 运输 |
室温;可能会有所不同 |
||||||||||||
| SMILES |
O=C1C2=C(O)C(C/C=C(C)C)=C3C(C=CC(C)(C)O3)=C2OC=C1C4=CC=C(O)C=C4 |
||||||||||||
| 参考文献 |
|
||||||||||||
| 相关活性 小分子 |
天丰素 | 伊利司莫 | Adarotene | 杨梅素 | 血根碱 | 白桦脂酸 | 牛磺鹅去氧胆酸 | 宝藿苷 I | 木香烃内酯 | (20S)人参皂苷 Rh2 | 桦木醇 | 虎杖苷 | N1-(4-丁基-2-甲基苯基)乙酰胺 | 遍在蛋白异肽酶抑制剂I,G5 | [6]-姜酚 |
| 密度 | 1.3±0.1 g/cm3 |
|---|---|
| 沸点 | 632.3±55.0 °C at 760 mmHg |
| 熔点 | 189° (uncorr), 193° (corr) |
| 分子式 | C25H24O5 |
| 分子量 | 404.455 |
| 闪点 | 218.7±25.0 °C |
| 精确质量 | 404.162384 |
| PSA | 79.90000 |
| LogP | 7.62 |
| 蒸汽压 | 0.0±1.9 mmHg at 25°C |
| 折射率 | 1.628 |
| 储存条件 | ?20°C |
|
|
| 符号 |

GHS09 |
|---|---|
| 信号词 |
Warning |
| 危害声明 |
H410 |
| 警示性声明 |
P273-P501 |
| 危害码 (欧洲) |
N |
| 风险声明 (欧洲) |
50 |
| 安全声明 (欧洲) |
61 |
| 危险品运输编码 | UN 3077 9 / PGIII |
|
~%
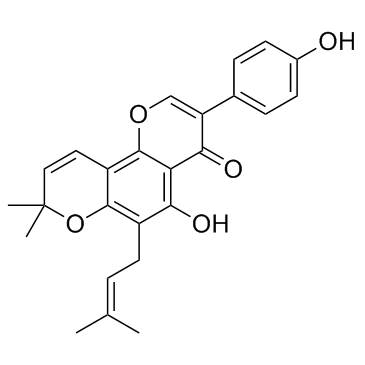
奥沙京
482-53-1
|
|
文献:Singhal, Ashok K.; Sharma, Ram P.; Thyagarajan, Gopalakrishna; Herz, Werner; Govindan, Serengolam V. Phytochemistry (Elsevier), 1980 , vol. 19, p. 929 – 934 |
| 奥沙京上游产品? 1 | |
|---|---|
|
|
|
| 奥沙京下游产品? 2 | |
|
|
|
|
Interactions of genistein and related isoflavones with lipid micelles. Langmuir 22(17) , 7175-84, (2006)
Genistein (5,7,4′-trihydroxyisoflavone) modulates the function of several transmembrane ion-channel proteins by mechanisms that are unrelated to phosphorylation events. Daidzein (7,4′-dihydroxy-isofla…
|
|
|
Electrochemical and spectrometric study of antioxidant activity of pomiferin, isopomiferin, osajin and catalposide. J. Pharm. Biomed. Anal. 48(1) , 127-33, (2008)
The antioxidant properties of pomiferin, isopomiferin, osajin and catalposide are evaluated. The electrochemical behaviour of these compounds at a carbon paste electrode was studied using square wave …
|
|
|
Pomiferin, histone deacetylase inhibitor isolated from the fruits of Maclura pomifera. Bioorg. Med. Chem. Lett. 17(17) , 4753-5, (2007)
The major constituents from the fruits of Maclura pomifera are the prenylated isoflavones, osajin (1) and pomiferin (2). Their structures were elucidated using NMR spectroscopic techniques and mass sp…
|
|
|
UNII-83R5N9X74B |
|
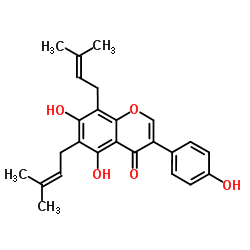
5-Hydroxy-3-(4-hydroxyphenyl)-8,8-dimethyl-6-(3-methyl-2-butenyl)-4H,8H-benzo[1,2-b:3,4-b']dipyran-4-one |
|
4H,8H-Benzo[1,2-b:3,4-b']dipyran-4-one, 5-hydroxy-3-(4-hydroxyphenyl)-8,8-dimethyl-6-(3-methyl-2-buten-1-yl)- |
|
5-Hydroxy-3-(4-hydroxyphenyl)-8,8-dimethyl-6-(3-methyl-2-buten-1-yl)-4H,8H-pyrano[2,3-f]chromen-4-one |
|
osajin |











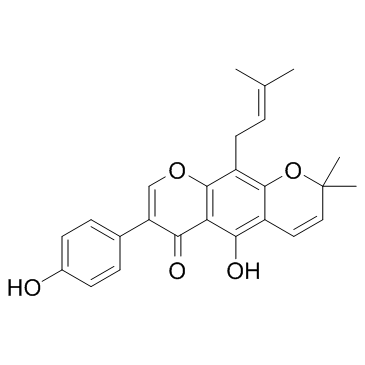
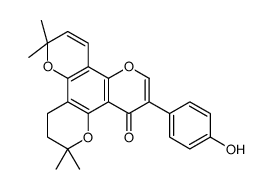
![5-methoxy-3-(4-methoxyphenyl)-8,8-dimethyl-6-(3-methylbut-2-enyl)pyrano[2,3-h]chromen-4-one结构式](https://www.chemsrc.com/caspic/443/5254-72-8.png)