This product was successfully added to cart!
品牌商品推荐
更多 >>商品详情
客户评价
| 描述 |
Coptisine 是从黄连中分离到的生物碱,是一种有效的非竞争性的 IDO 抑制剂,Ki 值为 5.8 μM,IC50 值为 6.3 μM。 |
||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 相关类别 |
|
||||||||||||
| 靶点 |
IDO:6.3 μM (IC50)
IDO:5.8 μM (Ki)
|
||||||||||||
| 体外研究 |
Coptisine是一种有效的非竞争性IDO抑制剂,Ki值为5.8μM,IC50值为6.3μM[1]。 Coptisine(0.1-100μM)抑制A549,H460,H2170,MDA-MB-231和HT-29细胞的增殖,IC50分别为18.09,29.50,21.60,20.15和26.60μM。 Coptisine(12.5,25,50μM)上调pH2AX和p21的表达,降低细胞周期蛋白B1,cdc2和cdc25C的表达,并以浓度依赖性方式诱导A549细胞的G2 / M阻滞和凋亡。 Coptisine(12.5,25,50μM)也诱导线粒体功能障碍并激活A549细胞中的半胱天冬酶活性。此外,Coptisine(50μM)以时间依赖性方式(0.5,1,2,4,12和24小时)增加ROS水平[3]。 |
||||||||||||
| 体内研究 |
Coptisine以浓度依赖性方式显示小鼠毒性增加,LD50值为880.18mg / kg。连环蛋白(154mg / kg /天,90天)对SD大鼠没有毒性。 Coptisine(23.35,46.7,70.05 mg / kg,po)剂量依赖性地降低TC,TG和LDL-c水平,并增加仓鼠血清中HDL-c含量至不同程度,减缓HFHC诱导的体重增加饮食,并在仓鼠中剂量依赖性地提高粪便中胆固醇和TBA的水平。 Coptisine(70.05 mg / kg,po)抑制HMGCR蛋白表达水平并诱导参与胆固醇代谢的SREBP-2,LDLR和CYP7A1的蛋白表达[2]。 |
||||||||||||
| 溶解度 |
体外:
在DMSO中10mM
|
||||||||||||
| 储备液 |
|
||||||||||||
| 细胞实验 |
将100mM浓度的Coptisine溶解在DMSO中,随后通过用细胞培养基稀释来制备浓度在100和0.1μM之间的浓度。在每次处理中使用的最终DMSO浓度小于0.1%。进行MTT测定以评估Coptisine的细胞增殖效应。简而言之,将2500个细胞/孔接种在含有补充有10%FBS和1%青霉素 – 链霉素的DMEM培养基的96孔板中。加入一系列Coptisine浓度并在5mM NAC存在或不存在下孵育48小时。温育48小时后,向每个孔中加入15μLMTT(5mg / mL)并在37℃下孵育4小时。然后,除去上清液并向每个孔中加入150μLDMSO以溶解晶体。通过Spectramax M4读板仪在595nm处测量吸光度[3]。 |
||||||||||||
| 动物实验 |
小鼠[2]在昆明小鼠上测试黄连碱的急性毒性,每组10只小鼠(每只雄性和雌性一半)。将Coptisine溶解于蒸馏水中,制备8个剂量(482.5,579,694,833,1,000,1,200,1,440和1,728mg / kg)给药。口服给药后,观察每只小鼠的反应,包括死亡率,并记录1周,以获得Coptisine的LD50值。大鼠[2]将40只SD大鼠分成对照组和Coptisine组(每只雄性和雌性的一半),处理90天。通过人体等效剂量(HED)和体表面积(BSA)归一化方法计算动物剂量。为了确定亚慢性毒性,使用对于成人(60kg)的最大HED of Coptisine(25mg / kg)作为参考,获得了Coptisine对SD大鼠(154mg / kg /天)的实际剂量。对照组大鼠给予相同体积的0.9%盐水。在整个实验中,给所有动物喂食正常饮食和随意饮水。每天记录大鼠的一般外观和行为,每10天测量一次体重,每天观察两次临床症状和死亡率。 |
||||||||||||
| 存储 |
请将产品存放在分析证书中的建议条件下。
|
||||||||||||
| 运输 |
室温;可能会有所不同 |
||||||||||||
| SMILES |
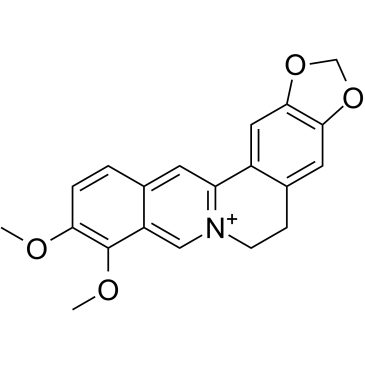
C1(C(CC[N+]2=C1C=C(C=C3)C(C4=C3OCO4)=C2)=C5)=CC6=C5OCO6 |
||||||||||||
| 参考文献 |
|
||||||||||||
| 相关活性 小分子 |
艾卡哚司他 | 吲哚莫德 | BMS-986205 | IDO-IN-7 | 盐酸黄连碱 | 那伏莫德 | 4-氨基-N-(3-氯-4-氟苯基)-N’-羟基-1,2,5-恶二唑-3-甲脒 | PF-06840003 | GNF-PF-3777 | IDO-IN-4 | 4-氨基-N-(3-溴-4-氟苯基)-N’-羟基-1,2,5-恶二唑-3-甲脒 | IDO-IN-12 | IDO-IN-2 | IDO-IN-3 |
| 分子式 | C19H14NO4 |
|---|---|
| 分子量 | 320.32 |
| PSA | 40.80000 |
| LogP | -0.87 |
|
~%
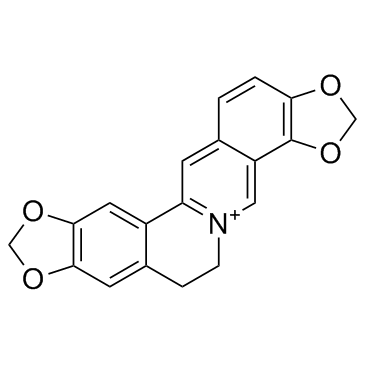
黄连碱
3486-66-6
|
|
文献:Natural Product Research, , vol. 28, # 7 p. 413 – 419 |
|
~%

黄连碱
3486-66-6
|
|
文献:Natural Product Research, , vol. 28, # 7 p. 413 – 419 |
|
~%

黄连碱
3486-66-6
|
|
文献:Chemical and Pharmaceutical Bulletin, , vol. 30, # 9 p. 3446 – 3449 |
|
6,7-Dihydrobis[1,3]benzodioxolo[5,6-a:4',5'-g]quinolizinium |
|
7,8,13,13a-Tetradehydro-2,3:9,10-bismethylenedioxyberbinium |
|
Coptisine |
|
Bis[methylenedioxy]protoberberine |
|
6,7-Dihydro[1,3]dioxolo[4,5-g][1,3]dioxolo[7,8]isoquino[3,2-a]isoquinolin-5-ium |
|
6,7-Dihydro[1,3]dioxolo[4,5-g][1,3]dioxolo[7,8]isoquinolino[3,2-a]isoquinolin-5-ium |
|
[1,3]Benzodioxolo[5,6-a]-1,3-benzodioxolo[4,5-g]quinolizinium, 6,7-dihydro- |
|
6,7-Dihydro[1,3]dioxolo[4,5-g][1,3]dioxolo[7,8]isochino[3,2-a]isochinolin-5-ium |
|
Coptisin |
|
coptisinium |
|
6,7-Dihydro[1,3]dioxolo[4,5-g][1,3]dioxolo[7,8]isoquino[3,2-a]isoquinoléin-5-ium |