This product was successfully added to cart!
品牌商品推荐
更多 >>商品详情
客户评价
| 中文名 |
2-溴-1-(4-氟苯基)-1-丁酮 |
|---|---|
| 英文名 |
N-(3-Fluoro-4-((6-methoxy-7-(3-morpholinopropoxy)quinolin-4-yl)-oxy)phenyl)-N-(4-fluorophenyl)cyclopropane-1,1-dicarboxamide |
| 中文别名 |
N-[3-氟-4-[[6-甲氧基-7-[[3-(吗啉-4-基)丙基]氧]喹啉-4-基]氧]苯基]-N-(4-氟苯基)环丙烷-1,1-二甲酰胺 |
| 英文别名 |
更多 |
| 描述 |
Foretinib是一种多靶点酪氨酸激酶抑制剂,抑制 Met 和 KDR 的IC50分别为0.4 nM 和 0.9 nM。 |
||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 相关类别 |
|
||||||||||||
| 靶点 |
KDR:0.9 nM (IC50)
c-Met:0.4 nM (IC50)
|
||||||||||||
| 体外研究 |
Foretinib抑制HGF受体家族酪氨酸激酶,Met的IC50值为0.4nM,Ron的IC50值为3nM。 Foretinib还抑制KDR,Flt-1和Flt-4,IC50值分别为0.9 nM,6.8 nM和2.8 nM。 Foretinib抑制B16F10,A549和HT29细胞的集落生长,IC50分别为40 nM,29 nM和165 nM [1]。最近的一项研究表明,Foretinib在胃癌细胞系MKN-45和KATO-III中对细胞生长的影响不同。 Foretinib抑制MKN-45细胞中MET和下游信号分子的磷酸化,而靶向KATO-III细胞中的GFGR2 [2]。 |
||||||||||||
| 体内研究 |
Foretinib(100 mg / kg,po)导致B16F10肿瘤Met和配体磷酸化的显着抑制(例如,HGF或VEGF)诱导肝脏中Met和Flk-1 / KDR的受体磷酸化,这两种情况持续24小时。 Foretinib(30-100mg / kg,每日一次,口服)导致肿瘤负荷减轻。用30和100mg / kg Foretinib治疗后肺表面肿瘤负荷分别减少50%和58%。携带B16F10实体瘤的小鼠的Foretinib治疗也分别导致30和100mg / kg的剂量依赖性肿瘤生长抑制为64%和87%。对于这两项研究,Foretinib的给药耐受性良好,没有明显的体重减轻[1]。 Foretinib被开发用于通过Met靶向HGF的异常信号传导并同时靶向参与肿瘤血管生成的几种受体酪氨酸激酶。 Foretinib在2至4小时内导致人异种移植物中的肿瘤出血和坏死,并且在96小时(每日5次剂量后)观察到最大的肿瘤坏死,导致完全消退[3]。 |
||||||||||||
| 溶解度 |
体外:
DMSO:≥38mg / mL(60.06 mM) * “≥”表示可溶,但饱和度未知。
|
||||||||||||
| 储备液 |
|
||||||||||||
| 激酶实验 |
使用三种测定形式之一研究激酶抑制:[33P]磷酸转移,荧光素酶偶联化学发光或AlphaScreen酪氨酸激酶技术。使用XLFit.33P-磷酸转移激酶试验通过非线性回归分析计算IC 50。反应在384孔白色透明底部高结合微量滴定板中进行。在含有40μg/ mL底物(聚(Glu,Tyr)4:1,22.5mM Na 2 CO 3,27.5mM NaHCO 3,50mM NaCl的50μL体积的包被缓冲液中,用2μg/孔的蛋白质或肽底物包被平板。 3mM NaN3。在室温(RT)下孵育过夜后,用50μL测定缓冲液洗涤涂覆的板一次。将测试化合物和酶与33P-γ-ATP(3.3μCi/ nmol)组合,总体积为20μL。将反应混合物在室温下孵育2小时并通过抽吸终止。随后用0.05%Tween-PBS缓冲液(PBST)洗涤微量滴定板6次。加入闪烁液(50μL/孔)并测量33P。使用MicroBeta闪烁计数器进行液体闪烁光谱测定。荧光素酶偶联化学发光测定法在384孔白色中等结合微量滴定板中进行反应。第一步,将酶和化合物合并,孵育60分钟;通过加入反应开始反应ATP和p肽底物(聚(Glu,Tyr)4:1)在20μL的最终体内,并在室温下孵育2-4小时。激酶反应后,加入20μL等份的Kinase Glo,并使用Victor平板读数器测量发光信号。 ATP总消耗量限制在50%。 AlphaScreenTM酪氨酸激酶试验使用包被有链霉抗生物素蛋白和包被有PY100抗磷酸酪氨酸抗体的受体珠的供体珠。生物素化的聚(Glu,Tyr)4:1用作底物。通过在供体 – 受体珠复合物形成后通过发光添加供体/受体珠来测量底物磷酸化。将激酶和测试化合物合并并预孵育60分钟,然后在384孔白色中等结合微量滴定板中加入ATP和总体积为20μL的生物素化聚(Glu,Tyr)。将反应混合物在室温下温育1小时。通过添加10μL含有75mM Hepes,pH 7.4,300mM NaCl,120mM EDTA,0.3%BSA和0.03%Tween-20的15-30μg/ mL AlphaScreen珠悬浮液来淬灭反应。在室温下孵育2-16小时后,使用AlphaQuest读数器读板。 |
||||||||||||
| 细胞实验 |
将B16F10,A549和HT29细胞(每孔1.2×103)与软琼脂混合,并接种在含有10%FBS和EXEL-2880的96孔板上的基础琼脂层上。对于含氧量正常的条件,将板在21%氧气,5%CO 2和74%氮气中孵育(37℃)12至14天,而在低氧条件下孵育(37℃)在缺氧室中进行1 %氧气,5%CO2和94%氮气。在添加50%Alamar Blue和荧光检测后,在每种条件下评估菌落数。 |
||||||||||||
| 动物实验 |
在幼稚小鼠或携带B16F10肿瘤的小鼠中进行体内靶调节研究。通过口服强饲法以10mL / kg施用Foretinib或载体(0.9%生理盐水)。为了检查肝脏中的Met磷酸化,在收获前10分钟静脉内施用HGF(10μg/小鼠)。为了检查肺中的Flk-1 / KDR磷酸化,在收获前30分钟静脉注射VEGF(10μg/小鼠)0.5小时后。通过免疫印迹分析确定受体磷酸化分析。 |
||||||||||||
| 存储 |
|
||||||||||||
| 运输 |
室温;可能会有所不同 |
||||||||||||
| SMILES |
O=C(NC1=CC=C(C(F)=C1)OC2=C3C=C(C(OCCCN4CCOCC4)=CC3=NC=C2)OC)C5(CC5)C(NC6=CC=C(C=C6)F)=O |
||||||||||||
| 参考文献 |
|
||||||||||||
| 相关活性 小分子 |
尼达尼布 | 1,3-二氢-3-[(3,5-二甲基-1H-吡咯-2-基)亚甲基]-2H-吲哚-2-酮 | 甲磺酸阿帕替尼 | N-[2-[4-(二乙氨基)丁基]氨基-6-(3,5-二甲氧基苯基)吡啶并[2,3-D-7-嘧啶基]-N’-(1,1-二甲基)脲 | 苯扎米特 | (2R)-1-[[5-[(Z)-[5-[[(2,6-二氯苯基)甲基]磺酰]-1,2-二氢-2-氧代-3H-吲哚-3-亚基]甲基]-2,4-二甲基-1H-吡咯-3-基]羰基]-2-(1-吡咯烷甲基)吡咯烷 | 3-四聚丙烯基二氢-2,5-呋喃二酮 | 利尼伐尼 | 西地尼布 | 6-[[7-[(1-氨基环丙基)甲氧基]-6-甲氧基-4-喹啉基]氧基]-N-甲基-1-萘甲酰胺 | RAF265 | 盐酸巴多昔芬 | BMS 777607 | SU14813 | 的Dihexa |
| 密度 | 1.4±0.1 g/cm3 |
|---|---|
| 沸点 | 828.5±65.0 °C at 760 mmHg |
| 分子式 | C34H34F2N4O6 |
| 分子量 | 632.654 |
| 闪点 | 454.8±34.3 °C |
| 精确质量 | 632.244629 |
| PSA | 116.45000 |
| LogP | 5.12 |
| 蒸汽压 | 0.0±3.0 mmHg at 25°C |
| 折射率 | 1.649 |
|
~86%
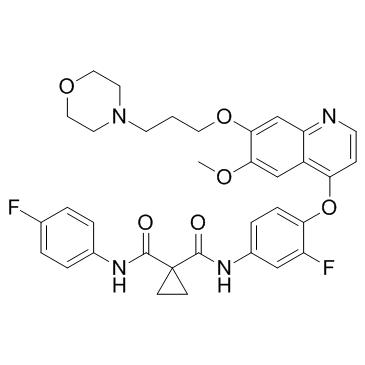
Foretinib
849217-64-7
|
|
文献:WO2011/9095 A1, ; Page/Page column 18-20 ; WO 2011/009095 A1 |
|
~70%

Foretinib
849217-64-7
|
|
文献:WO2005/30140 A2, ; Page/Page column 209 ; WO 2005/030140 A2 |
|
~81%

Foretinib
849217-64-7
|
|
文献:US2010/81805 A1, ; Page/Page column 13-14 ; |
| Foretinib上游产品? 4 | |
|---|---|
|
|
| Foretinib下游产品? 0 | |
|
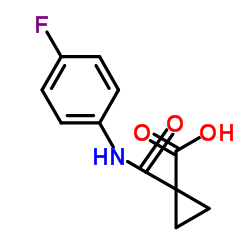
4-(4-(o-Methoxyphenyl)piperazinyl)-1-(3,4,5-trimethoxyphenyl)-1-butanol dihydrochloride |
|
1-Butanol,4-(4-(o-methoxyphenyl)piperazinyl)-1-(3,4,5-trimethoxyphenyl)-,dihydrochloride |
|
4-[4-(2-methoxyphenyl)piperazin-1-yl]-1-(3,4,5-trimethoxyphenyl)butan-1-ol dihydrochloride |
|
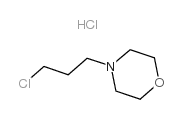
1,1-Cyclopropanedicarboxamide, N-[3-fluoro-4-[[6-methoxy-7-[3-(4-morpholinyl)propoxy]-4-quinolinyl]oxy]phenyl]-N’-(4-fluorophenyl)- |
|
EXEL-2880 |
|
4-(4-Hydroxy-4-(3,4,5-trimethoxyphenyl)butyl)-1-(o-methoxyphenyl)piperazine dihydrochloride |
|
N-[3-fluoro-4-([6-(methyloxy)-7-[(3-morpholin-4-ylpropyl)oxy]quinolin-4-yl]oxy)phenyl]-N’-(4-fluorophenyl)cyclopropane-1,1-dicarboxamide |
|
Foretinib |
|
N1-{3-fluoro-4-[(6-(methyloxy)-7-{[3-(4-morpholinyl)propyl]oxy}-4-quinolinyl)oxy]phenyl}-N1′-(4-fluorophenyl)-1,1-cyclopropanedicarboxamide |
|
N-[3-Fluoro-4-({6-methoxy-7-[3-(4-morpholinyl)propoxy]-4-quinolinyl}oxy)phenyl]-N’-(4-fluorophenyl)-1,1-cyclopropanedicarboxamide |











![3-Fluoro-4-{[6-methoxy-7-(3-morpholinopropoxy)-4-quinolyl]oxy}-aniline结构式](https://www.chemsrc.com/caspic/243/479690-10-3.png)
![N1'-[3-fluoro-4-[(7-hydroxy-6-methoxy-4-quinolyl)oxy]phenyl]-N1-(4-fluorophenyl)cyclopropane-1,1-dicarboxamide结构式](https://www.chemsrc.com/caspic/233/849217-50-1.png)